2. 山东大学第二医院耳鼻喉科, 山东 济南 250033 ;
3. 淄博市中心医院耳鼻喉科, 山东 淄博 255031
2. Department of Otolaryngology, The Second Hospital of Shandong University, Jinan 250033, Shandong, China ;
3. Department of Otolaryngology, Central Hospital of Zibo, Zibo 255031, Shandong, China
变应性鼻炎(allergic rhinitis,AR)是一种发生在鼻黏膜的、由IgE介导的、继发于抗原暴露的非感染性慢性炎性疾病,全球有近6亿人患有这种疾病[1-2]。虽然变应性鼻炎通常不会危及生命,但鼻塞、鼻痒等典型症状会严重影响患者的睡眠、工作和学习,慢性病程和反复发作的特点也带来了沉重的经济负担[3]。AR目前尚无法彻底治愈,变应原特异性免疫疗法(allergen specific immunotherapy,ASIT)是惟一的对因治疗手段,可以达到良好控制症状、改善生活质量、阻止疾病进展的目的[4]。1911年,皮下免疫治疗(subcutaneous immunotherapy,SCIT)被首次应用于花粉症,取得了良好的效果[5]。如今,SCIT已成为治疗变应性疾病的一线疗法之一。最新的变应性鼻炎诊疗指南(2015,天津)明确给出了SCIT的适应证、禁忌证、安全性和有效性,充分肯定了SCIT的临床价值[6]。但相比于药物治疗,免疫治疗的应用范围仍不够广泛[7]。此外,AR是哮喘发病的独立危险因素,40%的AR患者可合并支气管哮喘,而关于免疫治疗对鼻炎和哮喘的疗效对比研究数量较少。本研究通过2年的标准化皮下免疫治疗,观察尘螨疫苗对变应性鼻炎及支气管哮喘的有效性和安全性,同时评估单一尘螨制剂对多重过敏患者的疗效。
1 材料与方法 1.1 病例资料本组病例为2012年12月至2014年12月间于淄博市中心医院耳鼻喉科就诊并接受皮下免疫治疗的变应性鼻炎患者,AR的诊断符合2009年武夷山标准[8]。完成2年治疗并纳入统计者共58例,5~53岁,中位数年龄11岁。所有患者或其监护人均在治疗开始前签署了知情同意书。
纳入标准:临床病史显示鼻炎症状与尘螨具有相关性;有变应性鼻炎的典型症状和体征;屋尘螨皮肤点刺试验阳性(风团直径≥3 mm,丹麦ALK);屋尘螨血清特异性IgE阳性(≥0.7 kU/L,瑞典CAP)。
排除标准:有严重的或未控制的哮喘,正在使用β受体阻滞剂或ACEI进行治疗,严重的心血管疾病,免疫系统疾病,恶性肿瘤,妊娠,鼻息肉,鼻窦炎,过去3年内接受过免疫治疗。
1.2 治疗方案所有患者均在门诊接受标准化尘螨疫苗(安脱达,丹麦ALK)皮下注射,分为剂量累加和剂量维持两个阶段进行。从20 SQ-U开始,每周注射1次,剂量依次递增:20、40、80、200、400、800、2 000、4 000、8 000、10 000、20 000、40 000、60 000、80 000、100 000 SQ-U,共计15周。从第16周开始,采用100 000 SQ-U剂量维持,逐渐延长间隔至每6周注射1次。每次注射后,患者至少在门诊观察30 min。
1.3 疗效评估 1.3.1 症状评分通过调查问卷的形式记录鼻部症状总分(total nasal symptoms score,TNSS)和哮喘症状总分(total asthma symptoms score,TASS)。TNSS对4个主要鼻部症状进行评分,包括鼻塞、鼻痒、喷嚏和流涕,每项0~3分(0分=无症状;1分=症状轻微,易于忍受;2分=症状明显,可以忍受;3分=症状影响日常生活和/或睡眠),总和即为TNSS。合并哮喘的患者还需另外记录“气促、咳嗽、喘息、胸闷”等哮喘症状评分,日间症状评分从0分(无症状)到5分(症状严重,以至不能工作及正常生活),夜间症状评分从0分(无症状)到4分(症状严重,无法入睡),计算日间及夜间哮喘症状总分即为TASS。
1.3.2 视觉模拟量表在治疗前和治疗后的第6、12、24个月,采用视觉模拟量表(visual analogue scale,VAS)对患者的综合过敏症状进行评分。患者在0~10 cm的标尺上划线标出相应的分值,0分代表没有过敏症状,10分代表过敏症状很严重。
1.3.3 生活质量在治疗前和治疗后的第6、12、24个月,采用鼻结膜炎生活质量调查问卷(rhinoconjunctivitis quality of life questionnaire,RQLQ)[9]和哮喘生活质量调查问卷(asthma quality of life questionnaire,AQLQ)[10]对患者的生活质量进行评估。RQLQ从7个方面(鼻部症状、眼部症状、非鼻/眼症状、行为、情感、活动、睡眠)对变应性鼻结膜炎患者的健康状态进行评估,分值为0~6分,0分为最好,6分为最差,分值越高,表明生活质量受损越严重。PRQLQ和ARQLQ分别是针对儿童和青少年的调查问卷。AQLQ从5个常受哮喘影响的方面(活动受限、哮喘症状、心理状况、对应激原的反应、对自身健康的关心)进行评价,采用7分评分法,1分为最差,7分为最好,分值越高,表明生活质量越好。PAQLQ和AAQLQ分别是针对儿童和青少年的调查问卷。
1.4 安全性评估记录发生的局部不良反应和全身不良反应。局部不良反应主要表现为注射部位红斑、瘙痒、肿胀等,轻微的局部不良反应不需要特殊处理,多可在24 h内自行消退[11]。全身不良反应是指注射后远离注射部位出现的症状,如全身性荨麻疹、鼻炎、哮喘、血管性水肿和过敏性休克等。全身不良反应分级采用中华医学会耳鼻喉头颈外科学分会鼻科学组2011年制订的评级标准[12]。
1.5 统计学处理采用SPSS 22.0统计软件对所得数据进行分析处理。对治疗前后各项指标进行非参数检验,计量资料以中位数(P25,P75)表示,组间比较采用Mann-Whitney U检验,以P <0.05为差异有统计学意义。
2 结 果 2.1 患者资料58例患者均按免疫治疗的标准化进程完成2年疗程,患者的基本资料见表 1。变应性鼻炎患者均对屋尘螨过敏,40%(23/58)的患者合并其他变应原过敏,最常见合并变应原是花粉,其次是交链孢霉菌;90%(52/58)的患者同时伴有支气管哮喘。
| 表 1 变应性鼻炎患者基本资料 Table 1 Demographic and clinical characteristics of patients |
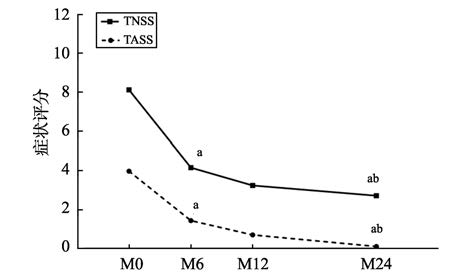
免疫治疗前后鼻部及哮喘症状评分的变化见图 1。在2年治疗期内,TNSS和TASS都呈持续性下降。治疗6、12、24个月后,鼻炎症状和哮喘症状均较治疗前显著好转,差异有统计学意义(P <0.05);治疗12个月后TNSS和TASS与治疗6个月时相比,差异无统计学意义(P> 0.05);治疗24个月后与治疗6个月时比较,TNSS和TASS的下降有统计学意义(P <0.05)。
各项鼻部症状的评分见表 2。在治疗开始前,流涕的症状评分最高,为3.00(2.00,3.00);在治疗结束时,喷嚏取得的疗效最好,为0.00(0.00,1.00)。治疗6个月后,四项鼻部症状都比治疗前有了显著改善,差异有统计学意义(P <0.05);而治疗24个月后与治疗6个月时相比,只有鼻塞症状评分的下降有统计学意义(P <0.05)。
|
图 1 鼻部及哮喘症状评分(中位数)在治疗前/M0、治疗6个月/M6、治疗12个月/M12、治疗24个月/M24的变化。与M0相比,aP <0.05;与M6相比,bP <0.05。 Figure 1 TNSS and TASS (median) pre- and post-treatment at 6,12 and 24 months. aP <0.05,difference from M0; bP <0.05,difference from M6. |
| 表 2 治疗前后鼻部症状评分[中位数(P25,P75)] Table 2 Individual nasal symptom scores (median ± IQR) pre- and post-treatment |
哮喘日间症状与夜间症状的评分见表 3。治疗前,哮喘日间症状评分高于夜间症状,分别为3.00(2.00,3.00)和1.00(1.00,2.00)。治疗6个月后,两组症状都比治疗前有了显著改善(P <0.05);治疗24个月后,哮喘日间症状和夜间症状评分都达到0.00(0.00,0.00),与治疗6个月时相比,差异有统计学意义(P <0.05)。
| 表 3 治疗前后哮喘症状评分[中位数(P25,P75)] Table 3 Asthma symptom scores (median±IQR) pre-and post-treatment |
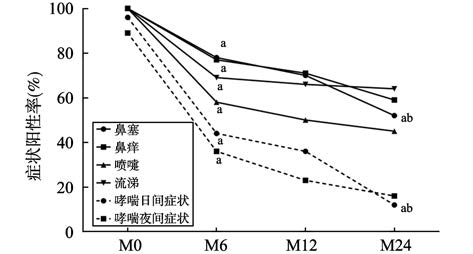
鼻部及哮喘症状阳性率的变化见图 2。治疗前,各项症状阳性率均接近100%,治疗6个月后,各项症状阳性率都比治疗前有了显著下降(P<0.05);治疗24个月后与治疗6个月时相比,只有鼻塞和哮喘日间症状阳性率的下降有统计学意义(P <0.05)。这与症状评分的变化基本吻合。
|
图 2 鼻部及哮喘症状阳性率在治疗前/M0、治疗6个月/M6、治疗12个月/M12、治疗24个月/M24的变化。与M0相比,aP <0.05;与M6相比,bP <0.05。 Figure 2 The positive rates of nasal symptoms and asthma symptoms pre- and post-treatment at 6,12 and 24 months. aP <0.05,difference from M0; bP <0.05,difference from M6. |
治疗前后鼻炎及哮喘综合症状的VAS评分变化见图 3。治疗前VAS评分为8.00(6.75,8.25),治疗2年后下降到2.00(1.00,3.00)。从M0到M6、M6到M12、M12到M24,VAS评分的下降均有统计学意义(P <0.05)。

|
图 3 VAS评分(中位数,四分位数)在治疗前/M0、治疗6个月/M6、治疗12个月/M12、治疗24个月/M24时的比较。*P <0.05。 Figure 3 Comparison of VAS scores (median±IQR) pre- and post-treatment at 6,12 and 24months.*P <0.05. |
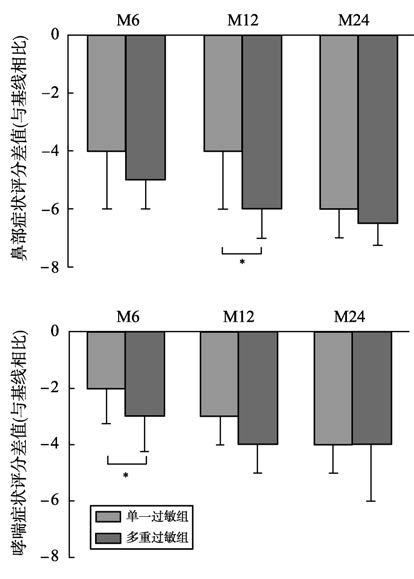
在治疗开始前,多重过敏患者的TNSS和TASS均显著高于单一过敏患者;治疗24个月后,两组患者的症状评分差异无统计学意义(表 4)。多重过敏患者症状评分的下降幅度大于单一过敏患者(图 4)。两组患者的鼻部症状评分,治疗12个月后评分差值出现显著差异(P<0.05);两组患者的哮喘症状评分,治疗6个月后评分差值即出现显著差异(P <0.05)。
| 表 4 单一过敏与多重过敏患者治疗前后鼻部及哮喘症状评分[中位数(P25,P75)] Table 4 TNSS and TASS (median±IQR) according to sensitization status pre- and post-treatment |
|
图 4 单一过敏与多重过敏患者在治疗6个月/M6、治疗12个月/M12、治疗24个月/M24时症状评分与基线差值(中位数,四分位数)的比较。*P <0.05。 Figure 4 Comparison of symptom scores change from baseline (median±IQR) according to sensitization status after 6,12 and 24months of treatment.*P <0.05。 |
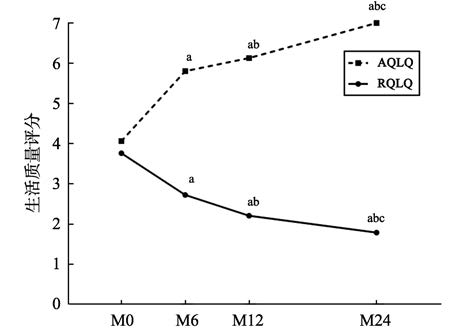
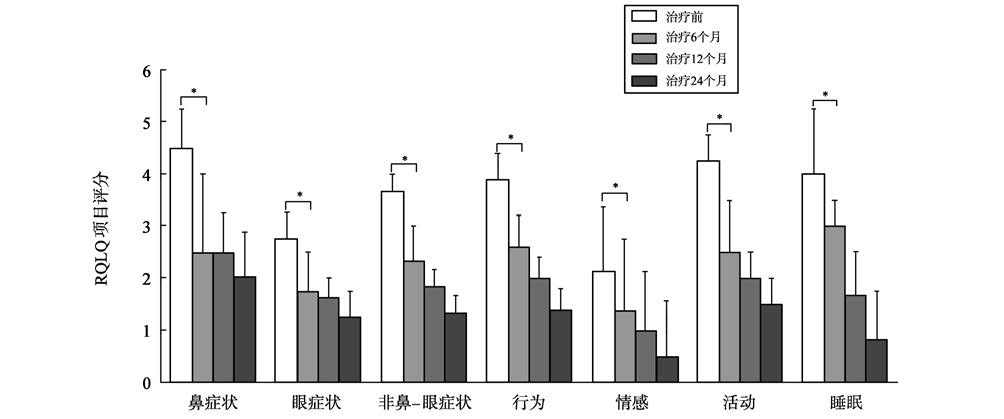
免疫治疗前后鼻炎和哮喘的相关生活质量变化见图 5。治疗6个月、12个月、24个月后,RQLQ评分从治疗前的3.90(3.20,4.30)逐渐下降到2.70(2.10,3.30)、2.20(1.70,2.70)和1.70(1.50,2.10),鼻结膜炎相关生活质量明显好转,各治疗时间点间差异显著(P <0.05)。AQLQ评分呈持续性上升,哮喘相关生活质量明显改善,各治疗时间点评分变化的差异有统计学意义(P <0.05)。治疗24个月后,AQLQ评分接近7,说明基本不存在由哮喘引起的生活质量损害。RQLQ各维度评分结果见图 6。治疗前鼻症状和活动2个维度评分最高,治疗24个月后,鼻症状评分仍最高,为2.0(1.0,3.0)。治疗6个月后,所有7个维度的生活质量都有了显著好转(P <0.05),并在治疗期内持续改善。
|
图 5 RQLQ和AQLQ评分(中位数)在治疗前/M0、治疗6个月/M6、治疗12个月/M12、治疗24个月/M24的变化。与M0相比,aP <0.05;与M6相比,bP <0.05;与M12相比,cP <0.05。 Figure 5 RQLQ and AQLQ (median) pre- and post-treatment at 6,12 and 24 months. aP <0.05,difference from M0; bP <0.05,difference from M6; cP <0.05,difference from M12. |
|
图 6 RQLQ各项目评分(中位数,四分位数)在治疗前、治疗6个月、治疗12个月、治疗24个月时的比较。*P <0.05。 Figure 6 Comparison of RQLQ domains scores (median±IQR) pre- and post-treatment at 6,12 and 24 months. *P <0.05. |
58例患者共进行了1 740次变应原注射。发生的局部不良反应大多可自行消退,无需特殊治疗。16例患者出现全身不良反应25次,全身不良反应发生率为1.4%,其中1级反应20次,占全身反应的80%,2级反应5次,占全身反应的20%,未出现严重全身不良反应或过敏性休克。口服抗组胺药和/或雾化吸入糖皮质激素治疗后,所有患者的症状均得到缓解。
3 讨 论近年来,变应性鼻炎的发病率逐步提高,给患者本人和社会都带来了沉重的负担。尘螨是我国常见的吸入性变应原,在儿童早期暴露于屋尘螨致敏原是继发哮喘的一个危险因素[13]。目前,AR的防治体系包括:避免接触变应原、药物治疗、变应原特异性免疫治疗和患者教育4个部分[14]。然而,尘螨在生活环境中普遍存在,完全避免接触是很难做到的;药物治疗只能暂时控制症状,无法提供长期疗效;对AR合并支气管哮喘的治疗,更是临床实践中的难点。变应原特异性免疫治疗在变应性疾病的治疗体系中具有重要地位,因为其不仅可以预防AR发展为哮喘及预防新发致敏,而且在疗程结束后仍具有稳定的长期疗效。
近年来,关于SCIT临床疗效和作用机制的研究越来越多。在IgE被发现后,人们就在寻找能够衡量SCIT疗效的客观指标,然而,IgE水平的改变与临床症状的改善并不相关[15],目前疗效评估仍然主要通过主观评价进行,如症状评分和生活质量评分等。本研究采用了症状评分、VAS和生活质量评分作为疗效评价指标。
鼻部症状和哮喘症状在治疗6个月后就出现了显著改善,并在随后的时间里维持在较低水平(图 1),各项症状阳性率的变化也呈同样的趋势(图 2)。治疗24个月后,鼻塞、哮喘日间及夜间症状明显好于治疗6个月时,鼻塞和哮喘日间症状的阳性率也显著低于治疗6个月时,说明SCIT的疗效与其疗程密切相关,推荐SCIT疗程持续2年以上是有临床意义的[12]。
SCIT能显著改善哮喘症状,而鼻部症状的改善与哮喘症状相比,其好转程度稍低。治疗24个月后,哮喘症状得到良好控制(表 3,图 2),AQLQ几乎达到满分(图 5),而鼻部症状仍然存在(表 2,图 2),RQLQ评分也仍然较高(图 5)。这可能是由于鼻腔作为上呼吸道的门户,更易受到季节更替和温度变化的影响,进而出现鼻部症状。
采用单一尘螨制剂对单一过敏和多重过敏的患者进行24个月的治疗后,两组患者的鼻部症状和哮喘症状都得到显著改善,且组间差异无统计学意义(表 4)。这提示单一制剂对多重过敏同样有效,这可能是因为尘螨是起主要作用的变应原,也可能与尘螨和其他变应原之间存在的交叉反应相关[16]。两组患者的哮喘症状评分差值,比鼻部症状评分差值更早出现显著差异(图 4),可能与本组患者的哮喘症状控制更佳有关。
SCIT的安全性也是临床关注的焦点。国内多中心、大样本的临床调查显示,屋尘螨疫苗皮下免疫治疗的全身不良反应发生率为0.47%[17],本研究全身不良反应发生率(1.4%)较高的原因,可能是因为有较多的儿童患者和合并哮喘患者(表 1)。虽然有一定的不良反应存在,但当以正确的方式进行个体化治疗时,SCIT可以被认为是安全的。
综上所述,应用标准化尘螨疫苗进行皮下免疫治疗是一种安全、有效的治疗手段,特别适用于变应性鼻炎合并支气管哮喘的患者。但SCIT的疗程选择、疗效评价的客观指标和不良反应的预防等问题仍需要进一步的深入研究。
| [1] |
韩德民, 张罗, 黄丹, 等.
我国11个城市变应性鼻炎自报患病率调查[J]. 中华耳鼻咽喉头颈外科杂志 , 2007, 42 (5) : 378–384.
HAN Demin, ZHANG Luo, HUANG Dan, et al. Self-reported prevalence of allergic rhinitis in eleven cities in China[J]. Chin J Otorhinolaryngol Head Neck Surgery , 2007, 42 (5) : 378–384. (  0) 0)
|
| [2] |
Law M, Morris JK, Wald N, et al.
Changes in atopy over a quarter of a century, based on cross-sectional data at three time periods[J]. BMJ , 2005, 330 (7501) : 1187–1188.
DOI:10.1136/bmj.38435.582975.AE ( 0) 0)
|
| [3] |
Bousquet J, Khaltaev N, Cruz AA, et al.
Allergic rhinitis and its impact on asthma (ARIA) 2008 update[J]. Allergy , 2008, 63 (Suppl 86) : 8–160.
( 0) 0)
|
| [4] |
Pichler C E, Marquardsen A, Sparholt S, et al.
Specific immunotherapy with Dermatophagoides pteronyssinus and D. farinae results in decreased bronchial hyperreactivity[J]. Allergy , 1997, 52 (3) : 274–283.
DOI:10.1111/all.1997.52.issue-3 ( 0) 0)
|
| [5] |
Noon L.
Prophylactic inoculation against hay fever[J]. Int Arch Allergy Appl Immunol , 1953, 4 : 285–288.
DOI:10.1159/000228032 ( 0) 0)
|
| [6] |
中华耳鼻咽喉头颈外科杂志编辑委员会鼻科组, 中华医学会耳鼻咽喉头颈外科学分会鼻科学组.
变应性鼻炎诊断和治疗指南(2015年, 天津)[J]. 中华耳鼻咽喉头颈外科杂志 , 2016, 51 (1) : 6–24.
( 0) 0)
|
| [7] |
Canonica G W.
A survey of the burden of allergic rhinitis in Europe[J]. Allergy , 2007, 62 (Suppl) : 17–25.
( 0) 0)
|
| [8] |
中华耳鼻咽喉头颈外科杂志编委会鼻科组, 中华医学会耳鼻咽喉头颈外科学分会鼻科学组.
变应性鼻炎诊断和治疗指南(2009年, 武夷山)[J]. 中华耳鼻咽喉头颈外科杂志 , 2009, 44 (12) : 977–978.
( 0) 0)
|
| [9] |
Juniper E F.
Measuring health-related quality of life in rhinitis[J]. J Allergy Clin Immunol , 1997, 99 (2) : 742–749.
DOI:10.1016/S0091-6749(97)90000-2 ( 0) 0)
|
| [10] |
Juniper E F, Guyatt G H, Ferrie P J, et al.
Measuring quality of life in asthma[J]. Am Rev Resp Dis , 1993, 147 (4) : 832–838.
DOI:10.1164/ajrccm/147.4.832 ( 0) 0)
|
| [11] |
Cox L, Wallace D.
Specific allergy immunotherapy for allergic rhinitis: subcutaneous and sublingual[J]. Immunol Allergy Clin North Am , 2011, 31 (3) : 561–599.
DOI:10.1016/j.iac.2011.05.001 ( 0) 0)
|
| [12] |
中华耳鼻咽喉头颈外科杂志编委会鼻科组, 中华医学会耳鼻咽喉头颈外科学分会鼻科学组.
变应性鼻炎特异性免疫治疗专家共识[J]. 中华耳鼻咽喉头颈外科杂志 , 2011, 46 (12) : 976–980.
( 0) 0)
|
| [13] |
Sporik R, Holgate S T, Platts-Mills T A, et al.
Exposure to house-dust mite allergen (Der pI) and the development of asthma in childhood. A prospective study[J]. N Engl J Med , 1990, 323 (8) : 502–507.
DOI:10.1056/NEJM199008233230802 ( 0) 0)
|
| [14] |
中华耳鼻咽喉头颈外科杂志编辑委员会, 中华医学会耳鼻咽喉科学分会.
变应性鼻炎的诊治原则和推荐方案(2004年, 兰州)[J]. 中华耳鼻咽喉头颈外科杂志 , 2005, 40 (3) : 166–167.
( 0) 0)
|
| [15] |
Bousquet J, Braquemond P, Feinberg J, et al.
Specific IgE response before and after rush immunotherapy with a standardized allergen or allergoid in grass pollen allergy[J]. Ann Allergy , 1986, 56 (6) : 456–459.
( 0) 0)
|
| [16] |
孙劲旅, 陈军, 张宏誉.
尘螨过敏原的交叉反应性[J]. 昆虫学报 , 2006, 49 (4) : 695–699.
SUN Jinlu, CHEN Jun, ZHANG Hongyu. Allergenic cross-reactivity between house dust mites and other mites[J]. Acta Entomologica Sinica , 2006, 49 (4) : 695–699. (  0) 0)
|
| [17] |
Chen J, Li B, Zhao Y, et al.
A prospective multicenter study of systemic reactions in standardized specific immunotherapy for allergic rhinitis in China[J]. Am J Rrhinol Allergy , 2014, 28 (1) : e40–e44.
DOI:10.2500/ajra.2014.28.4005 ( 0) 0)
|
 2016, Vol. 30
2016, Vol. 30

