变应性眼病是临床最常见的一种眼部疾病[1]。变应性结膜炎的患病率在人群中达到15%~40%[2]。通常与变应性鼻炎或哮喘共同出现[3]。变应性结膜炎主要包括:季节性变应性结膜炎(seasonal allergic conjunctivitis,SAC)、常年性变应性结膜炎(perennial allergic conjunctivitis,PAC)、春季卡他性角结膜炎(vernal keratoconjunctivitis,VKC)、特应性角结膜炎(atopic keratoconjunctivitis,AKC)以及通常与角膜接触镜的佩戴或人工角膜相关的巨乳头结膜炎(giant papillary conjunctivitis,GPC)等。
1 发病机制及症状和体征 1.1 SAC和PACSAC和PAC是最常见的两种变应性结膜炎。人群中的患病率达15%~20%[4],在美国95%的变应性结膜炎为这2种类型[5]。SAC和PAC主要是IgE介导的超敏反应,早期反应在临床上可持续20~30 min[6]。肥大细胞脱颗粒也可以激活血管内皮细胞,从而表达趋化因子及黏附分子,如内皮细胞黏附分子(intercellular adhesion molecule, ICAM)、血管细胞黏附分子(vascular cell adhesion molecule, VCAM)等。这些因素启动结膜炎症细胞的募集阶段,最终导致迟发型超敏反应[7]。
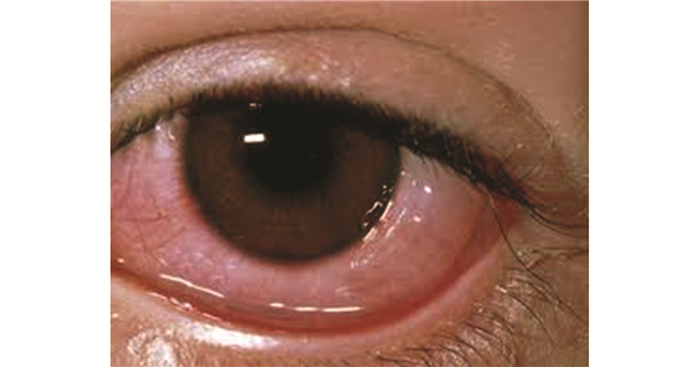
SAC和PAC的症状和体征基本一致。二者的主要区别在于变应原不同。SAC通常由空气中的花粉等引起,症状和体征多出现于春季或夏季,在秋冬季节通常缓解。PAC全年均可发生。SAC和PAC的主要症状包括眼痒、眼红、结膜水肿。眼红,也就是结膜充血的表现,一般为轻到中度[6]。结膜水肿通常为中度,一般比眼红的症状更显著。SAC和PAC通常不累及角膜。
|
图 1 季节性变应性结膜炎,结膜充血水肿 Figure 1 Seasonal allergic conjunctivitis: conjunctival hyperemia and edema |
VKC在气候温暖的地区或天气温暖的季节常见,通常分为角膜缘型、睑板型和混合型。多发生于男性患者,男女比例约为3:1[8]。80%的VKC发生于10岁左右男童,持续4~8年,在青春期前后逐渐缓解。通常双侧起病,有时也可单眼受累[9]。印度的一项大型研究结果表明,大多数患者发病的平均年龄为12岁,超过20岁以上发病的人数仅占12%[10]。VKC通常是由非特异性刺激如风、灰尘及阳光等引起的非特异性超敏反应。因此,此类患者血清中常见变应原的IgE检测结果通常为阴性[11]。目前认为,VKC是一种Th2淋巴细胞介导的慢性过敏性炎症,为Ⅳ型超敏反应。IL-4和IL-13可以通过诱导细胞外基质的产生和成纤维细胞的产生而导致形成巨乳头改变[7]。
临床表现主要包括眼痒、畏光、黏稠分泌物、异物感。VKC的主要体征包括角膜缘部乳头形成,有时乳头表面可覆盖白色分泌物,呈现一种凝胶状增厚的表现,称为Horner Trantas斑。VKC特征性的表现主要是角膜缘症状及上睑结膜铺路石样巨乳头。长期存在的角膜缘处巨乳头可导致角膜缘干细胞减少从而产生角膜新生血管。严重者可产生角膜缘赘生物从而影响视力,也可出现角膜瘢痕、圆锥角膜和盾形溃疡等[12]。并发症主要有:角膜瘢痕、新生血管、激素导致的青光眼及白内障、弱视、干眼、圆锥角膜等。
1.3 AKCAKC是特应性皮炎眼部并发症最严重的一种表现。Guglielmetti等[13]将其定义为:一种慢性的非感染性炎症,可以出现在特应性皮炎患者病程的任何时间,与特应性皮炎的严重程度无关。AKC的发病率呈升高趋势,若不及时治疗,可能致盲。AKC通常在20岁左右发病,直到40~50岁。
|
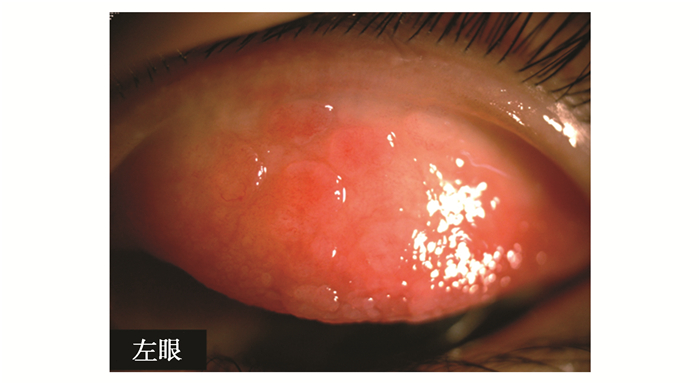
图 2 春季卡他性结膜炎,上睑结膜铺路石样乳头增生 Figure 2 Vernal keratoconjunctivitis: cobblestone-like papillary hyperplasia on the upper tarsal conjunctiva |
|
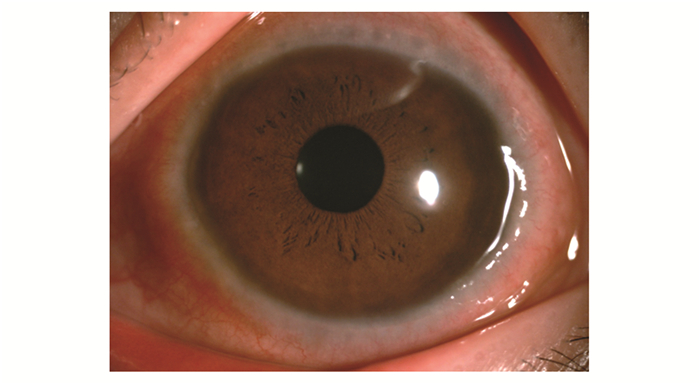
图 3 春季卡他性结膜炎,角膜缘全周胶样增生 Figure 3 Vernal keratoconjunctivitis: gelatinous swellings on corneal limbus |
主要症状包括眼痒、流泪、烧灼感、眼痛、眼红、视物模糊等,症状通常都是慢性的,没有季节性的规律。AKC患者的眼周和眼睑部可出现严重的湿疹。如果同时伴有色素沉着,则称作“熊猫眼”[13]。有时也可出现眼眶下部线性的褶皱,称为“Dennie-Morgan线”。通常累及双侧结膜,有结膜的增厚和充血,可有乳头增生,累及上下睑结膜,以下睑结膜为主[14]。除了慢性炎症介质的影响,由增厚发炎的睑结膜和不规则睑缘引起的外伤可以导致浅层角膜点状病变和点状角膜破损[13]。随着时间的推移,角膜病变可演变成磨损、溃疡、以及黏液斑和上皮丝状物的形成。长期炎症反应造成的角膜瘢痕及新生血管可导致失明。Power等[15]的一项对20例患者进行3年以上随访的研究发现,70%的AKC患者会有显著的角膜病变,其中60%有角膜新生血管、25%有穹隆缩短、20%有睑球粘连、有超过50%的患者需要行穿透性角膜移植。特应性反应可造成睑板腺功能障碍,泪膜不稳定,杯状细胞丢失及结膜鳞状上皮化生等[14]。AKC的其他并发症包括眼部的金黄色葡萄球菌定植,也易出现反复双侧单纯疱疹病毒的感染、白内障、圆锥角膜等[16]。

|
图 4 特应性结膜炎,右眼可见眼睑色素沉着及下睑Dennie-Morgan线 Figure 4 Atopic keratoconjunctivitis: pigmentation on the right eyelid and Dennie-Morgan line on the right lower eyelid |
GPC是一种以上睑结膜巨乳头增生为典型表现的炎症反应。外观上与VKC相似,但通常不累及角膜。引起巨乳头改变的刺激因素通常为惰性物质而非变应原,如角膜缘缝线、角膜接触镜、眼部假体及眼部皮样囊肿等。除去这些刺激因素,巨乳头改变也可消失。GPC患者结膜组织中也可出现肥大细胞、嗜碱性粒细胞、嗜酸性粒细胞等,但通常低于过敏反应水平。GPC患者的泪液中IgE及组胺等物质并不升高。
|
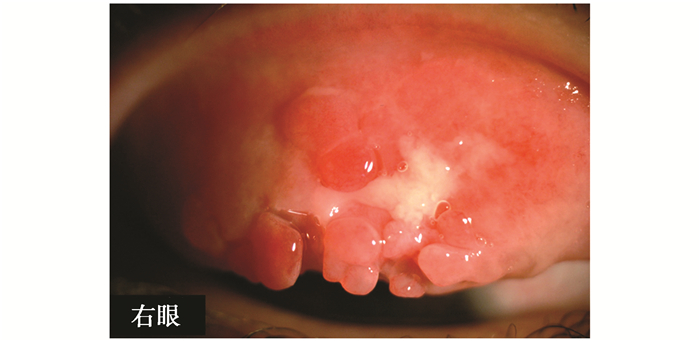
图 5 巨乳头性结膜炎,上睑可见巨大乳头 Figure 5 Giant papillary conjunctivitis: giant papillae on the upper tarsal conjunctiva |
变应性结膜炎的诊断主要依据病史、临床症状及体征,但实验室检查也可以起到辅助诊断的作用。
2.1 问诊为了做出明确诊断,应关注患者的以下情况:① 症状及体征(眼痒,眼红及球结膜水肿等);② 症状持续时间;③ 分泌物情况;④ 双侧或单侧发病;⑤ 角膜接触镜佩戴史;⑥ 过敏反应、哮喘、湿疹病史;⑦ 局部或全身用药史(如非处方滴眼液及全身用抗过敏药);⑧ 免疫抑制;⑨ 全身疾病(现有或曾患);⑩ 社会因素(吸烟、旅行及职业相关因素等)。
2.2 实验室检查主要包括:皮肤点刺试验、泪液中IgE测定、泪液细胞学检查及泪液中特异性蛋白质的检测等。
2.2.1 测定泪液中IgE总量方法有几种[17]:纸片放射吸附实验、免疫色谱法等。由于血泪屏障的存在,泪液中的IgE水平通常较低。健康人或非变应性结膜炎患者的泪液样本中IgE呈阴性。使用免疫吸收法,可发现VKC、AKC、SAC和PAC患者泪液中IgE浓度比正常人显著升高。可选用的试剂盒有Lacrytest、Allerwatch等。
Lacrytest是用与Schirmer's实验相同的方法,将试纸放在下穹隆部,试纸内抗IgE抗体释放,数分钟后即可得到结果。单条红线表示阴性结果,双条红线表示阳性结果。该实验的灵敏度和特异度分别可达91.7%和98.5%。Allerwatch[17]是一种新型的采用免疫层析法迅速测定泪液中IgE含量的实验室检查,根据Tatsuya等[18]的研究报道此方法的灵敏度和特异度分别为84.5%和97.5%,为目前主要泪液中IgE测定方法。
2.2.2 测定泪液中抗原特异性IgE含量[19]检测血清中抗原特异性IgE通常可用ELISA法或CAP放射免疫吸附法[17]。测定泪液中的抗原特异性IgE,每次需要至少50 μL的泪液,因此在泪液分泌不足的情况下,泪液样本的获取较困难。可选用的试剂盒有Immfast Check J1,可以检测泪液中香松木花粉、猫皮屑、尘螨的特异性IgE。此方法灵敏度和特异度分别为98.4%和97.7%。有研究表明,某些抗原特异性IgE只在泪液中存在。这个结果说明可能存在局部过敏反应。
2.2.3 泪液细胞学[17]可以用泪液、结膜刮片、刷片、印记细胞学或结膜活检等方法进行细胞学实验。只要在泪液中检测到嗜酸性粒细胞,即可高度怀疑过敏反应的存在,而未检测到嗜酸性粒细胞,也不能排除变应性结膜炎的诊断。变应性结膜炎患者泪液中还可存在中性粒细胞、淋巴细胞等。流式细胞学检查发现,VKC患者泪液中可存在Th2细胞。正常人体结膜内肥大细胞的数量在5 000~6 000个/mm3。在花粉流行季节,SAC患者当中肥大细胞中位数比正常人增加61%[20],在非花粉流行季节也相对较高。
2.2.4 泪液中特异性蛋白的监测过去5年间,有研究者用MALDI TOF质谱分析进行了泪液中蛋白质的质和量的分析[21]。大量在过去没有检测到的可能有病因学意义的蛋白质得到了定量分析。应用iTRAQ技术,研究者发现泪液中白蛋白、转铁蛋白、血液结合素等在VKC患者中的浓度为健康对照组的100倍[22]。研究评估了急性期蛋白血液结合素在泪液和结膜巨噬细胞内的浓度。血液结合素有清除和转运细胞外血红素的作用,而血红素的释放是为了在炎症反应期间保护细胞免受氧化性损伤。在活动期的VKC患者中,血红素的水平相对较高,同时与病情严重程度紧密相关。这项新的研究表明,将来有可能采用血液结合素来作为一种生化标志物,从而指导疾病的诊断和监测其进程。
Fujishima等[23]的实验表明,泪液中骨膜蛋白的含量可以测定,且其浓度升高对变应性结膜炎尤其是AKC有一定诊断价值。该实验首次证明泪液中骨膜蛋白可以测定并具有一定诊断价值。实验结果表明,泪液中骨膜蛋白含量在变应性结膜炎患者中有显著升高,浓度从高到低依次是AKC、VKC和SAC,可以反映出相应的泪液中IL-13的含量。研究人员认为该方法对AKC的诊断意义最大,VKC和SAC次之,但该实验中未涉及其他类型变应性结膜炎患者。
3 治疗 3.1 一般策略变应性结膜炎的治疗应依据病情的严重程度。对于轻症患者,主要应采取对患者进行宣传教育的方式。改变生活方式可从整体上帮助患者减轻症状[24]。避免接触变应原,在花粉流行季节尽量减少外出。对于角膜接触镜佩戴等引起的变应性结膜炎,可减少角膜接触镜的佩戴缓解症状。还包括以下措施:① 敏感患者应避免接触动物;② 使用低变应原的床上用品;③ 用热水洗床单,从而使某些抗原蛋白失活(如尘螨中的抗原);④ 睡前洗澡;⑤ 佩戴太阳镜,从而减少与空气传播变应原的接触;⑥ 避免揉眼,揉眼可使变应原接触眼表,从而引起过敏反应;⑦ 清洁眼睑;⑧ 冷敷,能够帮助缓解眼痒。
若生活方式改变已不足以控制疾病发展,可使用眼表润滑剂,如等张生理盐水、人工泪液及眼膏等来洗去眼表的变应原,但是这些药物对于炎症介质没有直接作用,只能暂时缓解症状,对中重度眼表过敏作用欠佳。这些药物也可能含有防腐剂,过度使用可对眼表造成进一步损害[24]。
3.2 药物治疗当前变应性结膜炎药物治疗主要有抗组胺药(酮替芬、氮卓斯汀、倍他司汀、依匹斯汀、奥罗他定及阿卡特定等),肥大细胞稳定剂(色甘酸、洛度沙胺、奈多罗米、哌罗来斯等),非甾体类抗炎药(NSAID),解充血药,糖皮质激素及免疫抑制剂等滴眼药。
3.2.1 抗组胺药主要作用是缓解瘙痒症状。抗组胺药可以加重甚至引起干眼症状[8],因此不适合长期应用。新型抗组胺药通常与肥大细胞稳定剂一起制成双效药。这种双效药被认为是目前主流的治疗变应性结膜炎药物。这类药物可以缓解眼红、充血、眼痒及眼部易激的症状。起效快,因此患者用药的依从性也更好。不良反应有刺痛、烧灼感、味苦、感冒症状、镇静等,通常较轻,可很快消失。此类双效制剂的代表药主要有0.25%阿卡他定(alcaftadine)及0.2%奥洛他定(olopatadine),用法为每天1次滴眼。其他此类药物有0.05%氮卓斯汀(azelastine)、1.5%贝托斯汀(bepotastine)、0.05%依匹斯汀(epinastine)、0.1%奥洛他定等,用法为每天1次滴眼。0.025%酮替芬(ketotifen)为该类药物的非处方药,每天2次滴眼[25]。若伴有全身其他过敏反应如变应性鼻炎、哮喘等情况可选用口服抗组胺药。
3.2.2 肥大细胞稳定剂发挥作用较抗组胺药慢,通常用于治疗轻到中度的症状。主要作用是抑制肥大细胞脱颗粒。通常用于治疗SAC和PAC,是轻度PAC的首选药物。这两种疾病的主要细胞类型为肥大细胞和嗜酸性粒细胞。肥大细胞稳定剂对早期和晚期的过敏反应均有效。
研究表明,NSAID药物(酮咯酸)的作用较奥洛他定差[26],主要用于缓解眼痒症状。然而,只有0.5%酮咯酸氨丁三醇得到美国FDA的批准用于SAC的治疗。现不作为变应性结膜炎一线用药。
3.2.3 糖皮质激素糖皮质激素类药物如利美索龙、氯替泼诺,一般作为最后的选择,通常用于疾病的急性期,短期使用,一般不超过1周。因为其可能造成结膜和角膜病毒感染的加剧,也可造成眼内压升高和白内障形成。新一代的糖皮质激素有一个重要的结构改变,在C20的位置上以一个酯结构取代了酮结构,从而使其代谢更快,也减少了一些不良反应。
3.2.4 免疫抑制剂免疫抑制剂如环孢素A、他克莫司(FK-506)、吡美莫司,能够抑制钙调磷酸酶,可用于代替糖皮质激素进行长期使用[27]。主要用于治疗VKC、AKC等严重类型的变应性结膜炎。研究表明,2%环孢素A对严重VKC有效,但对巨乳头增生疗效不佳[28]。环孢素A最常见的不良反应是烧灼感。低浓度环孢素A的此类不良反应较轻,但对其疗效的报道结果不一。Akpek等[29]的研究表明,对于激素抵抗AKC患者,应用0.05%环孢素A治疗4周后症状改善;而Daniell等[30]的研究结果显示,0.05%环孢素A与安慰剂相比,对AKC和VKC的疗效无明显差异。有报道称他克莫司可以减少特应性睑结膜炎患者结膜中的炎症细胞,尤其是嗜酸性粒细胞[31]。Vichyanond等[32]研究了10例难治性VKC,应用0.1%他克莫司眼膏4周后症状明显改善。有研究对比了0.1%他克莫司和2%环孢素A滴眼液的效果,发现二者均对VKC有效,但环孢素A的不良反应相对较重[33]。
3.3 变应原特异性免疫治疗(allergen-specific immunotherapy,SIT)SIT可用于治疗重症患者或有其他合并疾病如变应性鼻炎和/或哮喘的患者。将高剂量的抗原通过皮下注射或者舌下含服给药的方式,来降低人体对该抗原的敏感性[27]。
皮下免疫治疗(subcutaneous immunotherapy, SCIT)是一种相对较成熟的免疫治疗方式。SCIT剂量维持期一般需要每月给药一次,持续3年。作用可长达5~10年[8]。由于这种治疗方式存在发生全身过敏反应的风险,因此需在医生监督下给药,同时患者需经过筛选。全身反应的发生率较低,但也有致死的先例。有数据统计SCIT发生致死性全身过敏反应的概率约为1/2 000 000次注射,而接近死亡的全身过敏反应的发生率约为5.4次/1 000 000次注射[33]。在花粉流行季节对剂量进行调整可以减轻发生严重全身过敏反应的风险[34]。
舌下免疫治疗(sublingual immunotherapy, SLIT)是相对较新的一种免疫治疗方法。在美国和欧洲国家也越来越受青睐。Calderon等[35]发表的Meta分析结果显示,SLIT不仅可以改善患者眼红、眼痒等症状,还可以提高变应原的阈值。与SCIT相比,SLIT患者可以在家自行服药,没有注射的痛苦,发生全身过敏反应的概率也相对较低。但与SCIT的每月注射一次相比,SLIT需每日服药,需要患者有良好的依从性。2014年4月1日,美国FDA批准了法国Stallergenes公司的Oralair用于治疗花粉过敏。Oralair是一种含有五种草花粉的舌下含服免疫治疗制剂。后又批准了丹麦ALK-Abello公司的梯牧草花粉舌下含服片剂Grazax。
4 小结变应性结膜炎因其发病率较高,严重影响患者生活质量而越来越受到关注。其诊断和治疗手段也越来越多。变应性结膜炎的诊断主要依据患者的病史、症状和体征。泪液中IgE及各种特异性标志物的发现可以更加有助于明确诊断。变应性结膜炎的治疗应根据病情及类型首先对生活方式进行调整,远离或清除变应原是非常重要的。在传统药物如抗组胺药、肥大细胞稳定剂等的基础上,涌现出越来越多新型的有效药物。抗组胺药与肥大细胞稳定剂制成的双效制剂,已成为SAC和PAC的一线用药。对于严重的特殊类型的变应性结膜炎如VKC等可采用免疫抑制剂治疗。变应原免疫疗法因其对因、长效的特点也逐渐受到人们的关注。SCIT和SLIT各有利弊,但后者作为相对较新且较安全的新型疗法,有望在将来得到推广应用。
| [1] | La Rosa M, Lionetti E, Reibaldi M, et al. Allgergic conjunctivitis: a comprehensive review of the literature[J]. Ital J Pediatr, 2013, 39(1): 18. DOI:10.1186/1824-7288-39-18 |
| [2] | Rosario N, Bielory L. Epidemiology of allergic conjunctivitis[J]. Curr Opin AllergyClin Immunol, 2011, 11(15): 471–476. |
| [3] | Bousquet J, Khaltaev N, Cruz AA, et al. Allergic Rhinitis and its impact on Asthma(ARIA)2008 update(in collaboration with the World Health Oraganization, GA(2) LEN and AllerGen)[J]. Allergy, 2008, 63(Suppl 86): 8–160. |
| [4] | Wong AH, Barg SS, Leung AK. Seasonal and perennial conjunctivitis[J]. Recent Pat Inflamm Allergy Drug Discov, 2009, 3(2): 118–127. DOI:10.2174/187221309788489733 |
| [5] | Butrus S, Portela R. Ocular allergy:diagnosis and treatment[J]. Ophthalmol Clin North Am, 2005, 18(4): 1019–1032. |
| [6] | La Rosa M, Lionetti E, Reibaldi M, et al. Alllergic conjunctivitis:a comprehensive review of the literature[J]. Ital J Pediatr, 2013, 39: 18. DOI:10.1186/1824-7288-39-18 |
| [7] | Leonardi A, De Dominicis C, Motterle L. Immunopathogenesis of ocular allergy: a schematic approach to different clinical entities[J]. Curr Opin Allergy Clin Immunol, 2007, 7(5): 429–435. DOI:10.1097/ACI.0b013e3282ef8674 |
| [8] | Kari O, Saari KM. Diagnostics and new developments in the treatment of ocular allergies[J]. Curr Allergy Asthma Rep, 2012, 12(3): 232–239. DOI:10.1007/s11882-012-0252-9 |
| [9] | Leonardi A, Lazzarini D, Motterle L, et al. Vernal Keratoconjunctivitis-like disease in adults[J]. Am J Ophthalmol, 2013, 155(5): 796–803. DOI:10.1016/j.ajo.2012.11.018 |
| [10] | Saboo US, Jain M, Reddy JC, et al. Demographic and clinical profile of vernal keratoconjunctivitis at a tertiary eye care centre[J]. Indian J Ophthalmol, 2013, 61(9): 486–489. DOI:10.4103/0301-4738.119431 |
| [11] | Jun J, Bielory L, Raizman MB. Vernal conjunctivitis[J]. Immunol Allergy Clin North Am, 2008, 28(1): 59–82. DOI:10.1016/j.iac.2007.12.007 |
| [12] | Sangwan VS, Jain W, Vemuganti GK, et al. Vernal keratoconjunctivitis with limbal stem cell deficiency[J]. Cornea, 2011, 30(5): 491–496. DOI:10.1097/ICO.0b013e3181cbf9d3 |
| [13] | Guglielmetti S, Dart JK, Calder V. Atopic keratoconjunctivitis and atopic dermatitis[J]. Curr Opin Allergy Clin Immunol, 2010, 10(5): 478–485. DOI:10.1097/ACI.0b013e32833e16e4 |
| [14] | Bielory B, Bielory L. Atopic dermatitis and keratoconjunctivitis[J]. Immunol Allergy Clin North Am, 2010, 30(3): 323–326. DOI:10.1016/j.iac.2010.06.004 |
| [15] | Power WJ, Tugal-Tutkun I, Foster CS. Long-term follow-up of patients with atopic keratoconjunctivitis[J]. Ophthalmol, 1998, 105(4): 637–642. DOI:10.1016/S0161-6420(98)94017-9 |
| [16] | Joseph J, Chen MD, Danielle S, et al. Atopic keratoconjunctivitis: A review[J]. J Am Acad Dermatol, 2014, 70(3): 569–575. DOI:10.1016/j.jaad.2013.10.036 |
| [17] | Leonardi A. Allergy and allergic mediators in tears[J]. Exp Eye Res, 2013, 117: 106–117. DOI:10.1016/j.exer.2013.07.019 |
| [18] | Mimura T, Usui T, Yamagami S, et al. Relation between total tear Ig E and severity of acute seasonal allergic conjunctivitis[J]. Curr Eye Res, 2012, 37(10): 864–870. DOI:10.3109/02713683.2012.689069 |
| [19] | Mimura T, Yamagami S, Kamei Y, et al. Specific IgE in tear fluid and features of allergic conjuntivitis[J]. Curr Eye Res, 2013, 38(9): 917–925. DOI:10.3109/02713683.2013.794248 |
| [20] | Anderson DF, MacLeod JD, Baddeley SM, et al. Seasonal allergic conjunctivitis is accompanied by increased mast cell numbers in the absence of leucocyte infiltration[J]. Clin Exp Allergy, 1997, 27(9): 1060–1066. DOI:10.1111/cea.1997.27.issue-9 |
| [21] | Leonardi A, Palmigiano A, Mazzola EA, et al. Identification of human tear fluid biomarkers in vernal keratoconjunctivitis using iTRAQ quantitative proteomics[J]. Allergy, 2014, 69(2): 254–260. DOI:10.1111/all.12331 |
| [22] | Pattnaik L, Acharya L. Acomprehensive review on vernal keratoconjunctivitis with emphasis on proteomics[J]. Life Sci, 2015, 128: 47–54. DOI:10.1016/j.lfs.2015.01.040 |
| [23] | Fujishima H, Okada N, Matsumoto K, et al. The usefulness of measuring tear periostin for the diagnosis and management of ocular allergic diseases[J]. J Allergy Clin Immunol, 2016, 138(2): 459–467. DOI:10.1016/j.jaci.2015.11.039 |
| [24] | O'Brien TP1. Allergic conjunctivitis: an update on diagnosis and management[J]. Curr Opin Allergy Clin Immunol, 2013, 13(5): 543–549. DOI:10.1097/ACI.0b013e328364ec3a |
| [25] | Mahvan TD, Buckley WA, Hornecker JR. Alcaftadine for the Prevention of Itching Associated with Allergic Conjunctivitis[J]. Ann Pharmacother, 2012, 46(7-8): 1025–1032. DOI:10.1345/aph.1Q755 |
| [26] | Yaylali V, Demirlenk I, Tatlipinar S, et al. Comparative study of 0.1% olopatadine hydrochloride and 0.5% ketorolac tromethamine in the treatment of seasonal allergic conjunctivitis[J]. Acta Ophthalmol Scand, 2003, 81(4): 378–382. DOI:10.1034/j.1600-0420.2003.00079.x |
| [27] | Kari O, Saari KM. Updates in the treatment of ocular allergies[J]. J Asthma Allergy, 2010, 3: 149–158. |
| [28] | Pacharn P, Vichyanond P. Immunomodulators for conjunctivitis[J]. Curr Opin Allergy Clin Immunol, 2013, 13(5): 550–557. DOI:10.1097/ACI.0b013e328364d86a |
| [29] | Akpek EK, Dart JK, Watson S, et al. A randomized trial of topical cyclosporine 0.05% in topical steroid-resistant atopic keratoconjunctivitis[J]. Ophthalmol, 2004, 111(3): 476–482. DOI:10.1016/j.ophtha.2003.05.035 |
| [30] | Daniell M, Constantinou M, Vu HT, et al. Randomised contraolled trial of topical ciclosporin A in steroid dependent allergic conjunctivitis[J]. Br J Ophthalmol, 2006, 90(4): 461–464. DOI:10.1136/bjo.2005.082461 |
| [31] | Virtanen HM, Reitamo S, Kari M, et al. Effect of 0.03% tacrolimus ointment on conjunctival cytology in patients with severe atopic blepharoconjunctivitis:a retrospective study[J]. Acta Ophthalmol Scand, 2006, 84(5): 693–695. DOI:10.1111/j.1600-0420.2006.00699.x |
| [32] | Labcharoenwongs P, Jirapongsananuruk O, Visitsunthom N, et al. A double-masked comparison of 0.1% tacrolimus ointment and 2% cyclosporine eye drops in the treatment of vernal keratoconjunctivitis in children[J]. Asian Pac J Allergy Immunol, 2012, 30(3): 177–184. |
| [33] | Amin HS, Liss GM, Bernstein DI. Evaluation of near-fatal reactions to allergen immunotherapy injections[J]. J Allergy Clin Immunol, 2006, 117(1): 169–175. DOI:10.1016/j.jaci.2005.10.010 |
| [34] | Vadlamudi A, Shaker M. New developments in allergen immunotherapy[J]. Curr Opin Pediatr, 2015, 27(5): 649–655. DOI:10.1097/MOP.0000000000000267 |
| [35] | Calderon MA, Penagos M, Sheikh A, et al. Sublingual immunotherapy for treating allergic conjunctivitis[J]. Cochrane Database Syst Rev, 2011, 7: CD007685. DOI:10.1002/14651858.CD007685.pub2 |
 2017, Vol. 31
2017, Vol. 31

