随着鼻内镜外科技术的快速发展,已经由早期的内镜鼻窦外科学逐步扩展至内镜鼻眼相关外科学和内镜鼻颅底外科学领域。垂体瘤手术、脑脊液鼻漏修补术等已经常规由内镜下经鼻腔完成,也获得了包括耳鼻咽喉科、神经外科、眼科等专业在内的认可。内镜颅底外科借助角度镜和辅助导航等设备,可以充分显露颅底区域重要的血管神经,部分取代了开放式手术。随着颅底外科解剖学研究的深入和新型颅底手术器械设备的研发,内镜颅底外科诊治的疾病谱也越来越广,经鼻内镜颅底手术的范围也涵盖了几乎整个前、中、后颅底及部分侧颅底。其所涉及到的侧颅底严格意义上应该属于侧颅底的偏中线部分区域,即旁中线颅底,包括鼻咽区、咽鼓管区、神经血管区及颞下区。该区域传统上的开放式手术 (包括面中掀翻、颌骨外旋等中线径路方式,或者颅面联合径路等手术) 都有创伤较大、术中出血多、深部结构辨认困难、容易残留、神经血管损伤重等缺陷,故逐渐有被扩大鼻内镜径路 (expanded endonasal approach, EEA) 手术取代的趋势[1-2]。经验丰富的术者甚至可以达到破裂孔、颈静脉孔区内侧和颈内静脉结节区[3]。国内张秋航等[4]已经将内镜技术运用到耳科学领域,并取得了很好的效果。
中线旁颅底手术径路最早由美国匹兹堡大学医学中心提出[5-6]。内镜下旁中线颅底手术需要术者熟悉该区域的解剖和具备娴熟的内镜下中线颅底手术经验,每位术者都有其独到的经验[7-9]。相应的基础解剖研究也有开展[11-13]。我们在既往的手术中,多以翼突为中心向外扩展,现将内镜经鼻翼突径路旁中线颅底手术总结如下。
1 翼突区是经鼻内镜下旁中线颅底手术通道的枢纽或核心内镜下以翼突为中心的中线旁颅底区域可以包括以下结构:向外可以到达上颌窦后壁-翼腭窝,外侧颞下窝,后外侧方的蝶窦外侧隐窝,后外上方的海绵窦、Meckle腔,翼管后方的颈内动脉外侧方区域,再往外侧可以到达岩尖区,向下可以到达咽鼓管圆枕为中心的岩斜坡区域、咽鼓管区域、外侧的咽旁间隙上部。对于中线颅底手术中,翼突解剖也可以起到辅助定位作用,尤其是处理巨大侵袭性垂体瘤、脊索瘤或颅咽管瘤、软骨肉瘤、骨肉瘤等多区域侵犯的占位病变时,翼管定位颈内动脉是一种不错的选择 (图 1)。翼管是翼管神经及伴行动脉出入的管道,蝶窦气化良好时其底壁外侧可见翼管隆突,由前外方向后内方走行,翼管后口开口于破裂孔,与颈内动脉后曲相邻。该区域的解剖要点结构有:翼突、翼突根、翼突内外侧板、翼管、圆孔、卵圆孔,这些结构相互构成参考标志,即便是颅底肿瘤将周边结构侵占或推移,这些结构之间的相互参考,仍然可以起到指示作用,尤其是对于重要的血管神经:颈内动脉、眼动脉、视神经、外展神经等。

|
图 1 白色箭头指示翼管走行,前方指向翼腭窝,后方指向颈内动脉的破裂孔区域 Figure 1 The white arrow indicates the pterygoid canal, its anterior is pointing to the pterygopalatine fossa, and its rear is pointing to the foramen lacerum |
由于鼻窦、颅底、眼眶解剖区域的结构复杂、相互沟通,占位性病变多种多样,包括炎性肉芽肿等良性炎症性病变;内翻性乳头状瘤、血管瘤、纤维血管瘤等良性肿瘤;亦包括淋巴瘤和各种恶性肿瘤。恶性肿瘤临床表现缺乏特异性,难以早期发现,而且肿瘤组织学类型繁多,病理分类困难,恶性居多,可见有上皮源性 (表皮样、非表皮样、神经外胚层)、间质源性 (脉管、肌肉、骨、软骨、淋巴等),神经来源肿瘤 (神经鞘膜瘤、神经纤维瘤)、胆脂瘤、腺样囊性癌、恶性多形性腺瘤、胆固醇性肉芽肿、晚期鼻咽癌扩散、脑膜脑膨出、颅底脑膜瘤、蝶骨骨化纤维瘤、横纹肌肉瘤、软骨肉瘤、骨肉瘤或者脊索瘤和巨大侵袭性垂体腺瘤等。
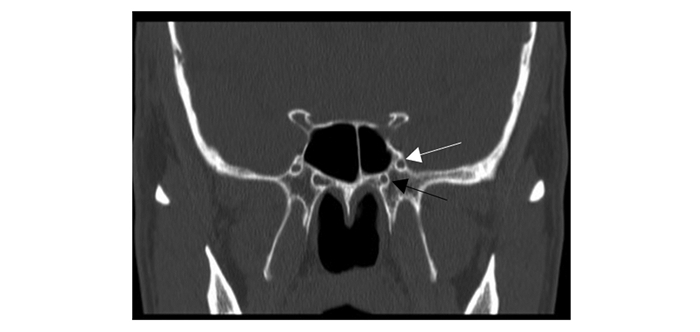
3 中线旁颅底区域的检查手段由于颅底疾病早期发现多困难,患者就诊时大多出现了眼科、神经科症状,此时的影像学检查多已经病变增大。过去偏重于鼻窦CT来检查鼻腔鼻窦疾病,如息肉、鼻窦炎、鼻窦良恶性肿瘤。对于颅底疾病,更侧重于颅底MR,常用的有平扫MR、增强MR以及动态增强MR,但不能仅仅局限于MR检查,对于某些疾病,辅之以常规颅底CT扫描,往往可以帮助临床诊断 (图 2),因为颅底固有的一些腔隙、孔道,两侧对称观察,可以发现侧颅底区域的一些疾病。颅底区域有助于诊断的自然孔道包括:圆孔——走行三叉神经第二支 (上颌神经),卵圆孔——走行三叉神经第三支 (下颌神经),棘孔——走行颌内动脉分支 (脑膜中动脉)。还有翼管神经后方指向破裂孔的上方,在影像上冠状位检查可以明确的寻找到翼管口与圆孔以及两者之间的固定关系 (图 3),这些都有助于该区域的疾病诊断。

|
图 2 A、B:鼻窦MR考虑翼腭窝、颞下窝区域占位,腺样囊性癌可能性大; C、D:CT扫描结合解剖对照,发现圆孔扩大; E:动态扫描曲线:平坦型。结合病史,考虑圆孔占位——神经来源可能性大,术后病理为圆孔区神经纤维瘤。 Figure 2 A, B: The paranasal sinuses MR imaging indicate that tumor was in the pterygopalatine fossa and infratemporal fossa and it might be the adenoid cystic carcinoma; C, D: CT scanning combined with anatomical study found that foramen rotundum was enlarged; E: The enhanced dynamic scanning curve indicated the platform type and considered the foramen rotundum occupancy from the nerve source.Postoperative pathology was the neurofibroma of the foramen rotundum. |
|
图 3 白色箭头:圆孔,黑色箭头:翼管。 Figure 3 White arrow, foramen rotundum;Black arrow, vidian canal. |
关于动态增强MR的临床意义[14-15],动态增强MR是一种无创的MR功能成像技术,可应用于鼻腔鼻窦、颅底、眼眶的占位性病变。通过各种定量、非定量参数量化分析血流灌注特征,提供常规MRI和MRA检查所不能获得的血流动力学方面的信息,无创性评价活体组织血管生成活性情况,反映相应病变组织的灌注、血管通透性、细胞外间隙容积等情况,动态观察病变的强化程度和方式,对进一步明确病变范围、病变良恶性的鉴别具有重要意义,越来越广泛的应用于肿瘤的诊断、治疗,判断疾病预后、预测复发率也具有一定作用,亦可应用于治疗后疗效评价等方面。术前获得尽可能详尽的病变信息,准确定位、定性,有助于治疗方法、手术方式的选择,改善患者的预后、提高生活质量。动态增强MR信号-时间曲线结果一般分三种类型(图 4):① 平坦型:见于良性病变;② 速升-平坦型:见于分化较好的恶性肿瘤和血流丰富的良性肿瘤;③ 速升-速降型:分化极差的恶性肿瘤。

|
图 4-1 动态增强MR信号-时间曲线 A: 速升-平坦型; B: 速升-速降型; C: 平坦型。 Figure 4-1 Dynamic enhancement MR signal-time curves A: Rapid rise-platform type; B: Downhill-platform type; C: Platform type. |

|
图 4-2 典型病例:女性79岁,增强MR中绿色图标显示与信号-时间曲线对应,瘤体不同部位均显示速升-平坦型曲线,病理结果为:蝶窦颅底高分化鳞状细胞癌。 Figure 4-2 Typical case of a 79-year-old female. The green icon displayed in the enhanced MR was corresponding to the signal-time curve. The different parts of the tumor showed a rapid rise-platform type curve. The pathological results: High differentiated squamous cell carcinoma of sphenoid sinus and skull base. |
内镜下经翼突径路旁中线颅底手术,虽然目前还没有一本教科书或手术指南来规定详尽的内镜下经鼻腔翼突径路旁中线颅底区域手术的步骤,但国内张秋航教授“内镜颅底外科学”一书中所述内镜下岩尖区、海绵窦以及翼腭窝、颞下窝手术中均述及需先磨除翼突后方能到达上述区域[16],国内外学者也将该解剖标志做了基础与临床的研究[17-19]。现将青岛大学附属医院鼻颅底外科处理该区域的临床经验总结如下。
4.1 鼻腔手术步骤① 充分收敛鼻腔:多以含有肾上腺素棉片放置鼻腔内,充分放置3次,不应以填塞的棉片数量为标准,而是在收敛的同时,将鼻腔内组织例如下鼻甲向外侧推移、中鼻甲向内侧推移,如有鼻中隔棘突,则沿棘突表面向偏曲对侧推移,目的是尽可能扩大鼻腔操作空间。② 处理中鼻甲:对于一般的中鼻甲可以推移,部分中鼻甲骨性部分肥厚者,则将中鼻甲沿上中1/3处向后剪除,注意尽量保持切除后中鼻甲黏膜完整,以便于保留中鼻甲黏膜瓣,利于术后小面积的颅底缺损的修补。
4.2 内镜下经翼突径路具体步骤见图 5。①切除钩突、暴露翼突根部:常规切除钩突,显露上颌窦,如欲采取带蒂鼻中隔黏 (骨) 膜瓣进行颅底修补术,可提前做移植瓣膜,将其旋转入上颌窦内放置备用,可以防止在后面的电钻磨除骨质的过程中将瓣膜误伤。也可以等离子刀切除钩突向后直至翼突根部黏膜,处理翼突根部的蝶腭孔,等离子需要沿血管纵行方向电凝形成血栓以充分止血,以颅底钻磨除翼突骨质直至根部,此时可能会有多次的颌内动脉分支出血,需耐心止血处理,也可以先将上颌窦后壁骨质磨除、显露翼腭窝处颌内动脉,沿动脉总干电凝止血。②磨除翼突根部后,显露翼管、外上方的圆孔及外侧的卵圆孔。根据病变位置,决定向外侧进入翼腭窝、颞下窝区域,还是向后外经蝶窦外侧隐窝进入中颅底,拟或是向后以翼管神经为标志,向后定位破裂孔上段颈内动脉,向后外进入海绵窦或Meckel腔等。磨除上颌窦后壁、开放翼腭窝时,在翼内外肌之间、脂肪组织内包含着颌内动脉走行,该处的脂肪组织可以预留,以便处理较小的颅底缺损。该处的血管如与病变无紧密关系,一般将其推移开即可,如果被病变包绕或粘连紧密,可行血管电凝烧灼断开,注意彻底止血,不可靠的电凝,往往可能造成术后大出血。颅底良性肿瘤,如神经鞘瘤等,多为颅内外沟通性肿瘤,因受周边结构限制,多采用囊内或瘤体内切除方式,逐渐缩小占位,松解周围粘连后再去除肿瘤;也可以沿着肿瘤占位效应产生的自然通道,由下向上切除,注意对正常神经的保护,以免术后出现面部、腭部或牙齿麻木等感觉[20-21]。对于鼻咽纤维血管瘤,其病变多隐匿在蝶骨大翼骨缝中[22-23],有时翼突根部是主要侵袭部位,需磨除肿瘤附着的骨性部分,对于Ⅲ期患者术中更应充分磨除颅底骨质,特别是翼管、圆孔及颅底松质骨,暴露至翼肌间隙的脂肪,降低术后复发率,部分肿瘤还需追踪到海绵窦内。由于该区域的血运相当丰富,所以针对较大的肿瘤,术前介入治疗封闭供应血管尤为重要,但是建议不要实施过于精确的分支血管封闭,我们的经验是:肿瘤主体可有数支血管供应,可以封堵其较大的主干。过于精细的分支供应阻断,术中还会有较多的其他交通分支的出血。
|
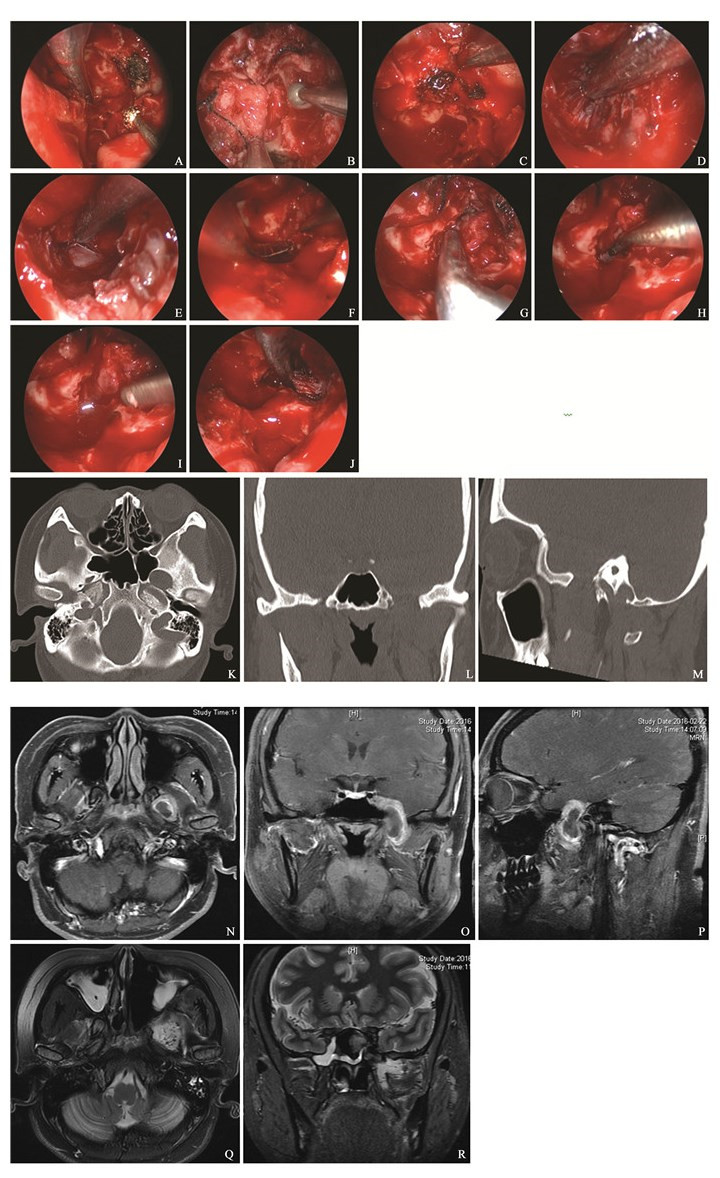
图 5 三叉神经第三支神经鞘膜瘤手术示意图 A: 磨除左侧翼突; B: 继续磨除至翼突根部; C: 椎板钳咬除翼腭窝骨壁; D: 分离翼腭窝内脂肪、翼内外肌; E: 显露颅外瘤体; F: 咬除蝶窦外侧隐窝骨壁; G: 显露颅内段瘤体; H: 由颅内向颅外剥离瘤体; I: 显露整个瘤体、去除; J: 去除瘤体后术腔; K~M:术前CT平扫,显示卵圆孔扩大; N~P: 术前MR,显示颅内外沟通性囊实性肿瘤; Q~R:术后MR:肿瘤切除干净。 Figure 5 Schematic diagram of the third branch schwannoma of the trigeminal nerve A: Grinded the left pterygoid process; B: Continue to grind the roots of pterygoid process; C: Removed the pterygopalatine fossa bone; D: Separated fat and pterygoid muscle; E: Revealed the extracranial tumors; F: Removed the lateral sphenoid sinus; G: Revealed the intracranial tumor; H: Separated the tumor from intracranial to extracranial; I: Revealed and removed the whole tumor; J: The operation cavity; K-M: Preoperative CT scan showed the foramen ovale enlargement; N-P: Preoperative MR scan show the intracranial and extracranial communicating cystic tumors; Q-R: Postoperative MR scan showed tumor total resection. |
典型病例:1例二次手术的鼻咽纤维血管瘤患者,第一次手术行颌内动脉栓塞术,第二次未行介入封堵,见图 6。
|
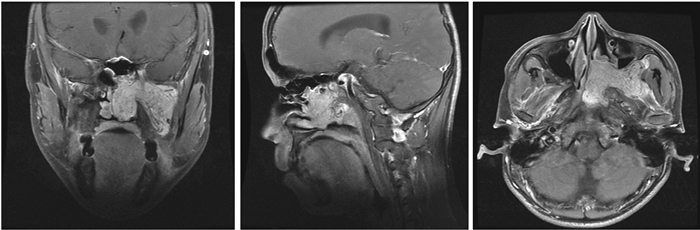
图 6-1 患者2015年1月18日第一次术前MR:左侧鼻咽、筛窦、翼腭窝、颞下窝占位。 Figure 6-1 The patient's first preoperative MR imaging on 18 Jan. 2015. Tumors in the left nasopharynx, ethmoid sinus, pterygopalatine fossa and infratemporal fossa. |
|
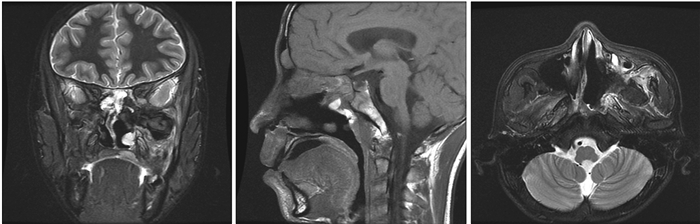
图 6-2 患者2015年2月3日第一次术后第一次复查MR:鼻咽部、翼腭窝、颞下窝未见异常信号。 Figure 6-2 The patient's first postoperative MR imaging on 3 Feb. 2015. No abnormal signal was found in the nasopharynx, pterygopalatine fossa and infratemporal fossa. |
|
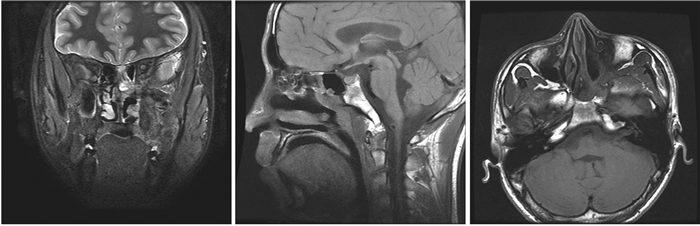
图 6-3 患者2016年1月27日第一次术后第二次复查MR:左侧鼻咽部组织增厚。 Figure 6-3 The patient's second review of MR imaging on 27 Jan. 2016. Left nasopharyngeal tissue was thickened. |
|
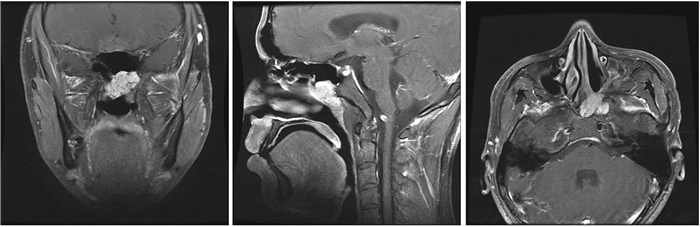
图 6-4 患者2017年2月15日第二次术前MR:左侧鼻咽顶后壁占位并突入左侧蝶窦。 Figure 6-4 The patient's second preoperative MR imaging on 15 Feb. 2017. Tumor in the left nasopharyngeal and sphenoid sinus. |
颅底解剖,术中影像导航、术中多普勒监测,双人四手操作,可靠的颅底修补,这些都是目前进行颅底中可以有效减少或避免严重并发症的措施。①解剖标志:翼突、翼突根、翼突内外侧板、翼管、圆孔、卵圆孔、咽鼓管圆枕,这些颅底骨性结构随着手术的进展而逐步显露,并且相互构成参考标志。有时视神经管、颈内动脉管以及二者之间形成的隐窝也可以作为手术参考标志。解剖标志应该根据术中需要,而不是全部寻找所有这些标志。即便是因为颅底肿瘤将周边结构侵占或推移,这些结构之间的相互参考,仍然可以起到指示作用,尤其是对于重要的血管神经:颈内动脉、眼动脉、视神经、外展神经等。②术前影像学检查:建议行颅底CT平扫+颅底MR+动态增强MR扫描,对于病变的侵犯范围、肿瘤的性质都有良好辅助作用。③导航是基于术前疾病占位影像检查,对于术中判定肿瘤周围重要血管神经以及是否切除干净有帮助,尤其是在关键部位比如紧邻颈内动脉、视神经等重要血管神经时,术中的影像辅助有助于辨别解剖位置、帮助术者树立信心[24-25]。但是对于肿瘤的占位效应,一旦切除、占位随之改变,即时的解剖关系变异可能会造成术者的安全界限假象,如为追求全切率,往往会带来严重或致命性后果,多普勒可以实时监控重要血管情况,在肿瘤占位效应改变时,探测到颈内动脉等大血管的血流声音,可以时刻提醒术者安全手术界限,防止重要血管损害。另外,严格意义上,对于牵涉到颅内神经的手术时,辅助神经检测也是非常有意义的,术中即时神经功能监测、判断病变或肿瘤侵及神经后功能保全与否,对于是否切除神经也是一种帮助。④双人四手操作:在手术开始时,即需要预留足够的操作空间。如进行右侧颅底手术,可以将鼻中隔后端骨质部分去除,助手在左侧鼻腔内操作吸引器,主刀则在右侧鼻腔内进行内镜和手术器械的操作 (如磨钻、咬钳等)。如果进行左侧颅底手术,或配合密切的助手,可以同一鼻腔内既有内镜、手术器械,也可以同侧吸引;为了保持术中视野的清晰,助手需要不定时的在内镜一侧进行鼻腔冲洗,这样一来可以始终保持镜头不被血液等沾污、保护视野清晰,同时还可以大大节约手术时间,关键时刻在处理比邻或包绕颈内动脉等重要血管的区域时,不间断的有效的吸引是手术得以完成的重要保障。双人四手操作法目前也已经是内镜颅底外科手术中的常规模式。但国内普遍进行的操作模式和国外有一定的区别,美国匹兹堡大学医学中心颅底外科的经典模式是由鼻科医生持镜和冲洗管、神经外科医生双手持手术器械,能够充分解放主刀双手,尤其在处理比邻颈内动脉、颅神经的病变时,主刀一手持吸引器、一手持手术钳等器械,极大方便了内镜下的操作,并有效解决主刀和助手器械反复“打仗”的局面。国内四手操作法,大多还是主刀左手持镜、右手持手术器械,助手持吸引器和冲洗管,不过多次磨合后,也一样能达到上述效果。⑤内镜颅底手术主要的担心就是颈内动脉和颅神经,尤其是视神经、动眼神经、外展神经以及三叉神经分支等,如何规避血管损伤?在以翼突为标志的内镜旁中线颅底手术中,充分磨除蝶窦前壁、显露外侧隐窝,气化好的蝶窦腔底壁有时可以显露翼管神经骨性隆起,保持翼管后内上方对应着颈内动脉破裂孔段这一假想线,尽量在其外侧进行。如进行海绵窦手术时,切开硬脑膜前可以穿刺以明确颈内动脉的位置,必要时先寻找到颈内动脉,以脑棉片等向内侧推移、给予术者一个操作空间,在明视下操作,就不会损伤到颈内动脉。在进行到颞下窝区域、Meckle腔区域时,注意以圆孔及其走行上颌神经、血管为内线,在外下方操作不要越过。对于侵及海绵窦的占位病变引起或者海绵窦出血时,应辨别是静脉出血还是颈内动脉主干或其分支的动脉出血。海绵窦的出血,助手在一侧鼻腔持续不间断的吸引 (以管径粗的吸引器管吸引) 是保持良好视野的前提,如短时间内不能完成手术,则应当妥善处理海绵窦出血,可以明胶海绵 (部分医院拥有流体明胶等) 局部按压片刻,多可以止血,可以继续操作。对于怀疑颈内动脉的出血,电凝并不都能达到良好的止血,及时以长纱条填塞止血、暂停手术并立刻颈内动脉介入栓塞是挽救的有效措施。术中导航联合多普勒反复检测重要血管,也是避免严重损害的不错选择。
7 颅底修复重建颅底手术无论是内镜下还是显微镜下抑或是开颅手术,切除病变后最关键一步就是颅底的修补。开放式进行颅底修补可以明视下进行,并能在硬膜内操作,修补切实可靠。内镜下颅底手术后,在狭窄的操作空间里进行操作,要求尽可能一次性修补到位。鼻腔因为天然的自体修补材料,如鼻甲黏膜瓣、鼻底黏膜瓣、鼻中隔带蒂或游离瓣膜,都可以作为修补的选择,可以做到因“鼻”制宜。对于较大的前、中、后颅底的缺损,如复发嗅母细胞瘤、巨大脊索瘤切除后,可选择帽状腱膜等组织,由额窦翻转铺到颅底,鼻腔侧需加固一层。对于旁中线颅底术后的缺损,面积往往不大,但因骨质结构沟壑纵横,不能达到一个理想的平铺面,这时需要以电钻等将缺损区周围骨质打磨出一个新鲜的较为平整的创面,制作移植床,再以鼻腔组织瓣或者股外侧阔肌筋膜、或肌浆等进行修补。
加强以翼突为解剖标志的内镜颅底手术,可以增加术中辨别的标志,并能以此为中心,向内、外扩展。翼突根部、翼管口、圆孔、卵圆孔、咽鼓管圆枕等是相对恒定的解剖关系,充分利用其空间定位,增加术者在操作中的空间立体感,有助于内镜颅底手术的扩展。
| [1] | DelGaudio JM. Endoscopic transnasal approach to the pterygopalatine fossa[J]. Arch Otolaryngol Head Neck Surg, 2003, 129(4): 441–446. DOI:10.1001/archotol.129.4.441 |
| [2] | Alfieri A, Jho HD, Schettino R, et al. Endoscopic endonasal approach to the pterygopalatine fossa: anatomic study[J]. Neurosurgery, 2003, 52(2): 374–378. DOI:10.1227/01.NEU.0000044562.73763.00 |
| [3] | 蒋卫红, 肖健云. 经鼻内镜颅底外科进展[J]. 中国耳鼻咽喉颅底外科杂志, 2015, 21(5): 351–353. |
| [4] |
张秋航, 丁秀勇, 王振霖.
单纯耳内镜下内听道听神经瘤切除[J]. 中华耳鼻咽喉头颈外科杂志, 2016, 51(10): 726–726.
ZHANG Qiuhang, DING Xiuyong, WANG Zhenlin. Exclusive endoscopic transsuprameatal approach for the pure intracanalicular acoustic neuroma[J]. Zhonghua Er Bi Yan Hou Tou Jing Wai Ke Za Zhi, 2016, 51(10): 726–726. DOI:10.3760/cma.j.issn.1673-0860.2016.10.002 |
| [5] | Kassam A, Snyderman CH, Mintz A, et al. Expanded endonasal approach: the rostrocaudal axis. Part Ⅰ.Crista galli to the sella turcica[J]. Neurosurg Focus, 2005, 19(1): E3. |
| [6] | Kassam AB, Gardner P, Snyderman C, et al. Expanded endonasal approach: fully endoscopic, completely transnasal approach to the middle third of the clivus, petrous bone, middle cranial fossa, and infratemporal fossa[J]. Neurosurg Focus, 2005, 19(1): E6. |
| [7] |
张秋航, 刘海生, 孔锋.
经鼻内镜岩斜坡及颞下窝肿瘤的外科治疗[J]. 中华耳鼻咽喉头颈外科杂志, 2005, 40(7): 488–492.
ZHANG Qiuhang, LIU Haisheng, KONG Feng. Endoscopic endonasal surgery for tumors of petroclival region and infratemporal fossa[J]. Zhonghua Er Bi Yan Hou Tou Jing Wai Ke Za Zhi, 2005, 40(7): 488–492. |
| [8] | Solari D, Villa A, De Angelis M, et al. Anatomy and surgery of the endoscopic endonasal approach to the skull base[J]. Transl Med UniSa, 2012, 2(5): 36–46. |
| [9] | 周兵, 黄谦, 崔顺九, 等. 内镜下经鼻泪前隐窝径路切除翼腭窝及颞下窝神经鞘瘤[J]. 中华耳鼻咽喉头颈外科杂志, 2013, 48(10): 802–806. DOI:10.3760/cma.j.issn.1673-0860.2013.10.003 |
| [10] | Jacquesson T, Berhouma M, Picart T, et al. Total removal of a trigeminal schwannoma via the expanded endoscopic endonasal approach. Technical note[J]. Acta Neurochir (Wien), 2015, 157(6): 935–938. DOI:10.1007/s00701-015-2409-5 |
| [11] |
于青青, 唐隽, 王跃建, 等.
旁中线颅底鼻内镜手术入路及其应用解剖学研究[J]. 中国医药科学, 2016, 6(22): 14–17.
YU Qingqing, TANG Jun, WANG Yuejian, et al. Lateral midline skull base transnasal endoscopic approach and its applied anatomy study[J]. Chin Med Sci, 2016, 6(22): 14–17. DOI:10.3969/j.issn.2095-0616.2016.22.005 |
| [12] | 沈鹏, 孙中武, 李建瑞, 等. 鼻内镜下经鼻径路解剖翼腭窝区临床观察[J]. 山东大学耳鼻喉眼学报, 2015, 29(2): 58–64. DOI:10.6040/j.issn.1673-3770.0.2014.328 |
| [13] | Hofstetter CP, Singh A, Anand VK, et al. The endoscopic, endonasal, transmaxillary transpterygoid approach to the pterygopalatine fossa, infratemporal fossa, petrous apex, and the Meckel cave[J]. J Neurosurg, 2010, 113: 967–974. DOI:10.3171/2009.10.JNS09157 |
| [14] | XIAN Junfang, DU Huarui, WANG Xinyan, et al. Feasibility and value of quantitative dynamic contrast enhancement MR imaging in the evaluation of sinonasal tumors[J]. Chin Med J (Engl), 2014, 127(12): 2259–2264. |
| [15] | Yuan Y, Yue XH, Tao XF, et al. The diagnostic value of dynamic contrast-enhanced MRI for thyroid tumors[J]. Eur J Radiol, 2012, 81(11): 3313–3318. DOI:10.1016/j.ejrad.2012.04.029 |
| [16] | 张秋航. 内镜颅底外科学[M]. 北京: 人民卫生出版社, 2013. |
| [17] |
刘剑锋, 韩军, 杨大章, 等.
内镜经翼突入路的解剖及其在处理颅底病变中的应用[J]. 中华耳鼻咽喉头颈外科杂志, 2015, 50(11): 909–914.
LIU Jianfeng, HAN Jun, YANG Dazhang, et al. Surgical anatomy, technique and application of endoscopic endonasal transpterygoid approach in skull base surgery[J]. Zhonghua Er Bi Yan Hou Tou Jing Wai Ke Za Zhi, 2015, 50(11): 909–914. DOI:10.3760/cma.j.issn.1673-0860.2015.11.006 |
| [18] | Fernandez-Miranda JC, Morera VA, Snyderman CH, et al. Endoscopic endonasal transclival approach to the jugular tubercle[J]. Neurosurgery, 2012, 71(1 Suppl Operative): 146–158. |
| [19] | Hofstetter CP, Singh A, Anand VK, et al. The endoscopic, endonasal, transmaxillary transpterygoid approach to the pterygopalatine fossa, infratemporal fossa, pettous apex, and the Meckel cave[J]. J Neurosurg, 2010, 113(5): 967–974. DOI:10.3171/2009.10.JNS09157 |
| [20] | Raza SM, Amine MA, Anand V, et al. Endoscopic Endonasal Resection of Trigeminal Schwannomas[J]. Neurosurg Clin N Am, 2015, 26(3): 473–479. DOI:10.1016/j.nec.2015.03.010 |
| [21] | Bresson D, McLaughlin N, Ditzel Filho LF, et al. Endoscopic endonasal approach for the treatment of schwannomas of the pterygopalatine fossa: Case report and review of the literature[J]. Neurochirurgie, 2014, 60(4): 174–179. DOI:10.1016/j.neuchi.2014.03.009 |
| [22] | Szymanska A, Szymanski M, Czekajska-Chehab E, et al. Two types of lateral extension in juvenile nasopharyngeal angiofibroma: diagnostic and herapeutic management[J]. Eur Arch Otorhinolaryngol, 2015, 272(1): 159–166. DOI:10.1007/s00405-014-2965-y |
| [23] | Rowan NR, Zwagerman NT, Heft-Neal ME, et al. Juvenile Nasal Angiofibromas: A Comparison of Modern Staging Systems in an Endoscopic Era[J]. J Neurol Surg B Skull Base, 2017, 78(1): 63–67. |
| [24] |
严波, 张秋航, 吕海丽, 等.
影像导航技术在内镜颅底外科中的应用[J]. 中华耳鼻咽喉头颈外科杂志, 2014, 49(9): 726–732.
YAN Bo, ZHANG Qiuhang, LÜ Haili, et al. Endoscopic skull base surgery under the guidance of image navigation technology[J]. Zhonghua Er Bi Yan Hou Tou Jing Wai Ke Za Zhi, 2014, 49(9): 726–732. |
| [25] | Battaglia P, Turri-Zanoni M, Lepera D, et al. Endoscopic transnasal approaches to pterygopalatine fossa tumors[J]. Head Neck, 2016, 38 Suppl 1: E214–220. |
 2017, Vol. 31
2017, Vol. 31

